二、EDTA配合滴定应用示例――水的总硬度测定
水的总硬度是指水中Ca2+、Mg2+的总含量。水中钙镁酸式碳酸盐形成的硬度称为暂时硬度,钙镁的其他盐类如硫酸盐、氯化物等形成的硬度称为永久硬度。暂时硬度和永久硬度的总和称为总硬度,其单位用每升水中含CaO或CaCO3的毫克数来表示,可写成CaOmg・L-1或CaCO3 mg・L-1。
操作步骤如下;
(一)配制0.01 mol・L-1的EDTA标准溶液
称取约0.19gEDTA二钠,用蒸馏水配成500ml溶液,然后用MgCO3作基准物质标定其浓度。
(二)EDTA溶液的浓度的标定
称取在110℃烘干过的基准物质MgCO30.21g(准至0.1mg),置于烧杯中,用稀盐酸溶解后配成250ml溶液,吸取25.00ml于锥形瓶中,加浓氨水至溶液呈碱性,再加5mlPH约为10的NH+-NH3・H2o 缓冲溶液,加铬黑T指示剂,用EDTA标准溶液滴定至溶液呈蓝色.
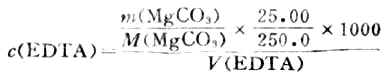
(三)水的总硬度测定
取水样50ml,加入5mlPH=10的NH+-NH3・H2O 缓冲溶液,再加铬黑T指示剂数滴,用0.01ml mol・L-1的EDTA标准溶液滴定至溶液呈蓝色。按下式计算出每升水中CaCO3的含量作为总硬度(单位mg・L-1)。
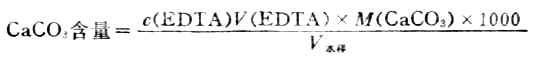
| 上一页:一、EDTA配合沆定的基本原理 |
| 当前页:二、EDTA配合滴定应用示例――水的总硬度测定 |
| 下一页:第一节 比色分析的基本原理 |