二、强酸弱碱盐溶液的PH值
一元强酸弱碱盐,例如NH4CL溶液中:
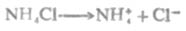
NH4+离子是NH3的共轭酸,它在水中电离:
或简写为 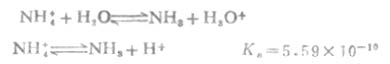
CL-离子不与水电离出的H+结合,它与溶液的酸碱性无关。可认为NH4+就是酸,与水作用放出H+而使溶液显酸性。当c/Ka≥500时,可用式(2-3)计算。
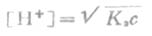
式中,c为浓盐酸的浓度。PH值可由[H+]计算。
多元强酸弱碱盐例如(NH4)2SO4溶液中PH值的计算,与一元强酸弱碱盐的PH值计算类似。
| 上一页:一、强碱弱酸盐溶液的PH值 |
| 当前页:二、强酸弱碱盐溶液的PH值 |
| 下一页:三、两性物质溶液的PH值 |