二、判断氧化还原反应进行的程度
氧化还原反应属可逆反应,同其他可逆反应一样,在一定条件下也能达到平衡。随着反应不断进行,参与反应的各物质浓度不断改变,其相应的电极电位也在不断变化。电极电位高的电对的电极电位逐渐降低,电极电位低的电对的电极电位逐渐升高。最后必定达到两电极电位相等,则原电池的电动势为零,此时反应达到了平衡,即达到了反应进行的限度。利用能斯特方程式和标准电极电位表可以算出平衡常数,判断氧化还原反应进行的程度。若平衡常数值很小,表示正向反应趋势很小,正向反应进行得不完全;若平衡常数值很大,表示正向反应可以充分地进行,甚至可以进行到接近完全。因此平衡常数是判断反应进行程度的标志。
氧化还原K与反应中两个电对的标准电极电位的关系为:
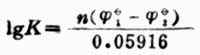
式中,n―反应中得失电子数;
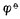
1―正反应中作为氧化剂的电对的标准电极电位;
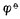
2―正反应中作为还原剂的电对的标准电极电位。
由式(6-4)可见,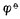
1与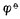
2之差值愈大,K值也愈大,反应进行得也愈完全。
例11 计算下列反应在298K时的平衡常数,并判断此的以应进行的程度。
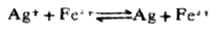
解: 电极反应Ag++e-→Ag 1=+0.7996V
1=+0.7996V
Fe2+→Fe3++e- 2=+0.77V
2=+0.77V
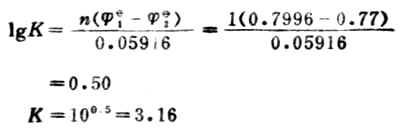
此反应平衡常数很小,表明此正反应进行得很不完全。
例12 计算下列反应的298K时的平衡常数,并判断此反应进行的程度。
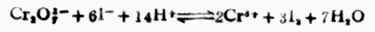
解:
电极反应 Cr2O72-+14H++6e-+→2Cr3+7H2O
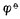
1=+1.33V
2I-→I2+2e- 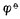
1=+0.535V
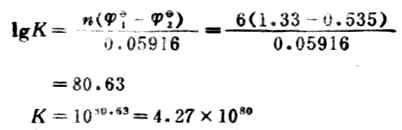
此反应的平衡常数很大,表明此正反应能进行完全,实际上可以认为能进行到底。
例13 向0.45mol.L-1铅盐溶液中加锡,发生下列反应,

计算298K时反应的平衡常数,达到反应限度时溶液中Pb2+浓度为多少。
解:
电极反应:Pb2++2e-→Pb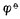
1=-0.1263V
Sn→Sn2++2e-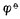
2=-0.1364V
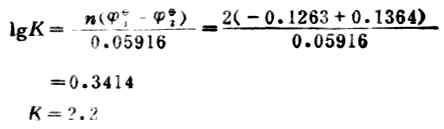
设平衡(达到反应限度)时溶液中Pb2+浓度为χmol.L-1。

χ 0.45-χ
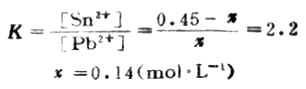
即达到反应限度时溶液中Pb2+浓度为0.14mol.L-1。
| 上一页:一、判断氧化还原反应自发进行的方向 |
| 当前页:二、判断氧化还原反应进行的程度 |
| 下一页:三、 电位法测定溶液的PH值 |