一、红细胞生理
1.红细胞的数量、形态和功能 红细胞(erythuocyte)是血液中数量最多的一种血细胞,正常男性每微升血液中平均约500万个(5.0×1012/L),女性较少,平均约420万个(4.2×1012/L).红细胞含有血红蛋白,因而使血液呈红色.红细胞在血液的气体运输中有极重要的作用.在血液中由红细胞运输的氧约为溶解于血浆的70倍;在红细胞参与下,血浆运输二氧化碳的能力约为直接溶解于血浆的18倍(详见第五章第三节).正常红细胞呈双凹圆碟形,平均直径约8μm,周边稍厚.这种细胞开头的表面积与体积之比,较球形时为大,因而气体可通过的面积也较大;由细胞中心到大部分表面的距离较短,因此气体进出红细胞的扩散距离也较短.这种形状也有利于红细胞的可塑性变形.红细胞在全身血管中循环运行,常要挤过口径比它小的毛细血管和血窦间隙,这时红细胞将发生卷曲变形,在通过后又恢复原状,这种变形称为塑性变形.表面积与体积的比值愈大,变形能力愈大,故双凹圆碟形红细胞的变形能力远大于异常情况下可能出现的球形红细胞.红细胞保持双凹圆碟形需要消耗能量。
红细胞膜是以脂质双分子层为骨架的半透膜。氧和二氧化碳等脂溶性气体可以自由通过,尿素也可以自由透入。在电解质中,负离子(如CI-、HCO3-)一般较易通过红细胞膜,而正离子却很难通过。红细胞内Na+ 浓度远低于细胞外,而细胞内K+浓度远高于细胞外,这种细胞内外的Na+、K+浓度差主要是依靠细胞膜上Na+泵的活动来维持的。低温贮存较久的血液,血浆内K+浓度升高,就是由于低温下代谢几乎停止,Na+泵不能活动的缘故。
红细胞结合和携带氧的过程并不消耗能量,血红蛋白中的Fe2+也不被氧化,若Fe2+被氧化成Fe3+成为高铁血红蛋白,即失去携氧能力。红细胞消耗葡萄糖,主要是通过糖酵解和磷酸戊糖旁路,所产生的能量(以结合于ATP的形式)主要是用于供应细胞膜上Na+泵的活动,用于保持低铁血红蛋白不致被氧化,也用于保持红细胞膜的完整性和细胞的双凹圆碟形。
2.红细胞比容 红细胞在血液中所占的容积百分比,称为红细胞比容(hematocritvalue),可以用分血计(hematocrit)来测定。通常是将一定量的血液与抗凝剂混匀,置于用直径2.5mm的平底玻璃管制成的分血计中,以每分钟3000转的速度离心半小时,使血细胞下沉压紧,即可测出红细胞比容。正常成年人的红细胞比容,男性为40%-50%,女性为37%-48%。但这是从手臂等处浅静脉抽血测定的数值,并且这时在压紧的红细胞之间有很少量血浆;同时,全身各类血管中,血液的红细胞比容值也不尽相同。
3.正常红细胞生成所必需的原料和其它因素 在幼红细胞的发育成熟过程中,细胞核的存在对于细胞分裂和合成血红蛋白有着重要的作用。在这些阶段,合成细胞核的主要构成物质―DNA必须有维生素B12和叶酸作为辅酶。
维生素B12是含钴的有机化合物,多存在于动物性食品中。机体对维生素B12的吸收必须要有内因子(intrinsic factor)和R结合蛋白(Rprotein)参与。内因子是由胃腺的壁细胞所分泌的一种糖蛋白,分子量在50000-60000之间,而R(rapid)蛋白是一种电泳速度很快的血浆蛋白。在酸性的胃液中,维生素B12主要与R蛋白结合,到了小肠上段处胰蛋白酶将这种结合断裂,维生素B12转而与内因子结合。内因子有两个活性部位,一个部位可与维生素B12结合,另一个部位则可与回肠上皮细胞膜上的特异受体结合。在正常情况下,内因子-B12复合物在小肠上段可保护维生素B12不受小肠内蛋白水解酶的破坏。当复合物运行至回肠段,便与回肠粘膜受体结合而被吸收进入门脉系统血流,一部分贮存在肝,一部分又与运输维生素B12的转钴蛋白Ⅱ(transcobalamineⅡ)结合,沿血液输送到造血组织,参与红细胞生成过程。当胃的大部分被切除或胃腺细胞受损伤,机体缺乏内因子,或体内产生抗内因子的抗体时,即可发生维生素B12吸收障碍,影响幼红细胞的分裂和血红蛋白合成,出现巨幼红细胞性贫血,即大细胞性贫血。
叶酸是以蝶酰单谷氨酸的形式吸收的。吸收之后,在双氢叶酸还原酶的催化下,形成四氢叶酸。存在于血浆中的叶酸几乎全是四氢叶酸的单谷氨酸盐。但进入组织细胞后,又通过酶促作用,再转变为多谷氨酸盐,才具有活性。叶酸缺乏时也引起与维生素B12缺乏时相似的巨幼红细胞性贫血。只是在维生素B12缺乏时,还可伴有神经系统和消化道症状。
合成血红蛋白还必须有铁作为原料,每亳升红细胞需要1mg铁,每天需要20-25mg铁用于红细胞生成,但人每天只需从食物中吸收1mg(约5%)以补充排泄的铁,其余95%均来自人体铁的再利用。机体贮存的铁主要来自于破坏了的红细胞。衰老的红细胞被巨噬细胞吞噬后,血红蛋白被消化而释出血红素中的Fe2+。这样释出的铁即与铁蛋白(ferritin)结合,此时的铁为Fe3+,聚集成铁黄素颗粒而沉淀于巨噬细胞内。血浆中有一种运铁蛋白(transferrin),可以来往运行于巨噬细胞与幼红细胞之间,以运送铁。贮存于铁蛋白中的Fe3+,先还原成Fe2+再脱离铁蛋白,而后与运铁蛋白结合。每分子运铁蛋白可以运送两个Fe2+,运送到幼红细胞后,又可反复作第二次运输。此外,还可以通过巨噬细胞与红母细胞直接接触,以提供合成血红蛋白所需的铁。由于慢性出血等原因,体内贮存的铁减少,或造血功能增强而供铁不够,均可引起小细胞性贫血,这主要是合成血红蛋白不足。此外,红细胞生成还需要氨基酸和蛋白质、维生素B6、B2、C、E,微量元素铜、锰、钴和锌等。
4.红细胞生成的调节 每个成年人体内约有25×1012个红细胞,每24小时便有0.8%的红细胞进行更新,也就是说每分钟约有160×106个红细胞生成;当机体有需要时,如失血或某些疾病使红细胞寿命缩短时,红细胞的生成率还能在正常基础上增加数倍。目前已经证明有两种调节因子分别调制着两个不同发育阶段红系祖细胞的生长。一种是早期的红系祖细胞,称为爆式红系集落形成单位(burst forming unit-erythroid,BFU-E),这是因为它们在体外培养中能形成很大的细胞集落,组成集落的细胞散布成物体爆炸的形状,这种早期祖细胞的生长和在体外形成集落都依赖于一种称为爆式促进因子(burst promoting activitor,BPA)的刺激作用。BPA是一类分子量为25000-40000的糖蛋白,以早期红系祖细胞BFU-E为作用的靶细胞,可能是促进更多的BFU-E从细胞周期中的静息状态(G0期)进入DNA合成期(S期),因而使早期祖细胞加强增殖活动。另一种是晚期的红系祖细胞,称为红系集落形成单位(colony forming unit-erythroid,CFU-E),它们在体外培养中只能形成较小的集落。晚期红系祖细胞对BPA不敏感,但主要接受促红细胞生成素(erythropoietin,EPO)的调节。促红细胞生成素是一种热稳定(80℃)的糖蛋白,分子量为34000。当组织中氧分压降低时,血浆中的促红细胞生成素的浓度增加,它促进红系祖细胞向前体细胞分化,又加速这些细胞的增殖,结果使骨髓中能合成血红蛋白的幼红细胞数增加,网织红细胞加速从骨髓释放。早在本世纪50年代,动物实验已显示了促红细胞生成素活性的存在,以后又确定促红细胞生成素主要由肾组织产生。切除双肾后,血浆中促红细胞生成素的浓度急剧降低。用分子生物学手段进一步证明,从肾组织细胞中已提取出编码促红细胞生成素的Mrna 和Cdna,还确定促红细胞生成素和mRNA和cDNA,还确定促红细胞生成素基因定位在7号染色体上。近年来有迹象提示人类的某些血液病,如再生障碍性贫血是红系祖细胞促红细胞生成素受体有缺陷所致(图3-2)。
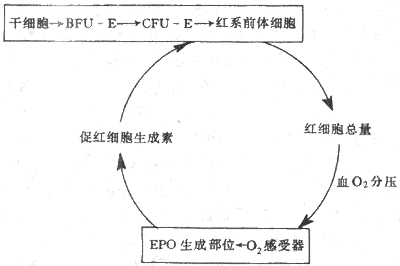
图3-2 EPOA调节红细胞生成的反馈调节环
促红细胞生成素主要由肾组织产生,但肾外,如肝脏,也有小量生成。晚期肾病患者,肾脏产生EPO已基本停止,但体内仍有小量EPO促使骨髓继续产生红细胞。
其他一些激素,包括雄激素、甲状腺激素和生长激素,都可增强促红细胞生成素的作用;雌激素则有抑制红细胞生成的作用。这可能是男性的红细胞数和血红蛋白量高于女性的原因。
| 上一页:第三节 血细胞及其功能 |
| 当前页:一、红细胞生理 |
| 下一页:二、白细胞生理 |