二、氨的代谢
(一)氨的来源
1.组织中氨基酸分解生成的氨 组织中的氨基酸经过联合脱氨作用脱氨或经其它方式脱氨,这是组织中氨的主要来源。组织中氨基酸经脱羧基反应生成胺,再经单胺氧化酶或二胺氧化酶作用生成游离氨和相应的醛,这是组织中氨的次要来源,组织中氨基酸分解生成的氨是体内氨的主要来源。膳食中蛋白质过多时,这一部分氨的生成量也增多。
2.肾脏来源的氨 血液中的谷氨酰胺流经肾脏时,可被肾小管上皮细胞中的谷氨酰胺酶(glutaminase)分解生成谷氨酸和NH3。
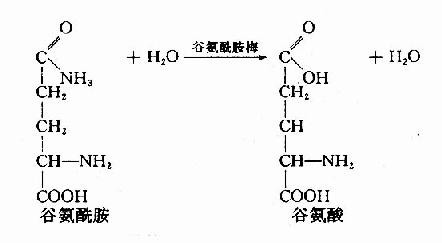
这一部分NH3约占肾脏产氨量的60%。其它各种氨基酸在肾小管上皮细胞中分解也产生氨,约占肾脏产氨量的40%。
肾小管上皮细胞中的氨有两条去路:排入原尿中,随尿液排出体外;或者被重吸收入血成为血氨。氨容易透过生物膜,而NH+4不易透过生物膜。所以肾脏产氨的去路决定于血液与原尿的相对pH值。血液的pH值是恒定的,因此实际上决定于原尿的pH值。原尿pH值偏酸时,排入原尿中的NH3与H+结合成为NH+4,随尿排出体外。若原尿的pH值较高,则NH3易被重吸收入血。临床上血氨增高的病人使用利尿剂时,应注意这一点。
3.肠道来源的氨 这是血氨的主要来源。正常情况下肝脏合成的尿素有15?0%经肠粘膜分泌入肠腔。肠道细菌有尿素酶,可将尿素水解成为CO2和NH3,这一部分氨约占肠道产氨总量的90%(成人每日约为4克)。肠道中的氨可被吸收入血,其中3/4的吸收部位在结肠,其余部分在空肠和回肠。氨入血后可经门脉入肝,重新合成尿素。这个过程称为尿素的肠肝循环(enterohepatin circulation of urea)。
肠道中的一小部分氨来自腐败作用(putrescence)。这是指未被消化吸收的食物蛋白质或其水解产物氨基酸在肠道细菌作用下分解的过程。腐败作用的产物有胺、氨、酚、吲哚、H2S等对人体有害的物质,也能产生对人体有益的物质,如脂肪酸、维生素K、生物素等。
肠道中NH3重吸收入血的程度决定于肠道内容物的pH值,肠道内pH值低于6时,肠道内氨生成NH+4,随粪便排出体外;肠道内pH值高于6时,肠道内氨吸收入血。临床上给高血氨病人作灌肠治疗时,禁忌使用肥皂水等,以免加重病情。
(二)氨的去路
氨是有毒的物质,人体必须及时将氨转变成无毒或毒性小的物质,然后排出体外。主要去路是在肝脏合成尿素、随尿排出;一部分氨可以合成谷氨酰胺和门冬酰胺,也可合成其它非必需氨基酸;少量的氨可直接经尿排出体外。尿中排氨有利于排酸。

图7-5 氨的来源和去路
(三)氨的转运
1.葡萄糖-丙氨酸循环:肌肉组织中以丙酮酸作为转移的氨基受体,生成丙酸经血液运输到肝脏。在肝脏中,经转氨基作用生成丙酮酸,可经糖异生作用生成葡萄糖,葡萄糖由血液运输到肌肉组织中,分解代谢再产生丙酮酸,后者再接受氨基生成丙氨酸。这一循环途径称为“丙氨酸椘咸烟茄贰?alanineglucose cycle)。通过此途径,肌肉氨基酸的NH2基,运输到脏脏以NH3或天冬氨酸合成尿素。(图7-6)
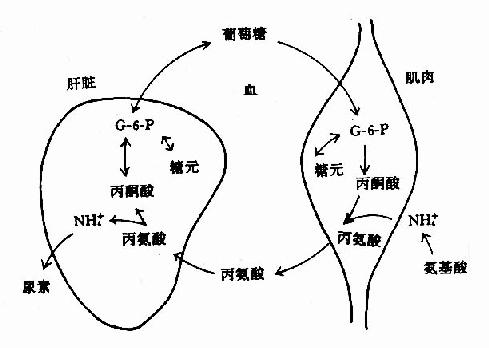
图7-6 葡萄糖丙氨酸循环
饥饿时通过此循环将肌肉组织中氨基酸分解生成的氨及葡萄糖的不完全分解产物丙酮酸,以无毒性的丙氨酸形式转运到肝脏作为糖异生的原料。肝脏异性生成的葡萄糖可被肌肉或其它外周组织利用。
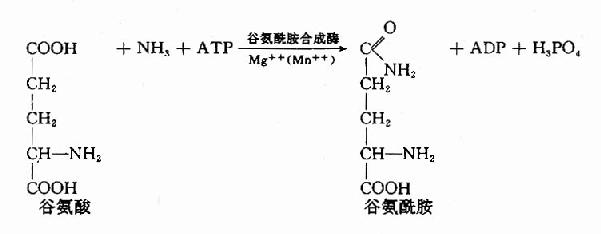
2.氨与谷氨酸在谷氨酰胺合成酶(glutamine synthetase)的催化下生成谷氨酰胺(glutamine),并由血液运输至肝或肾,再经谷氨酰酶(glutaminaes)水解成谷氨酸和氨。谷氨酰胺主要从脑、肌肉等组织向肝或肾运氨。
(四)尿素合成
根据动物实验,人们很早就确定了肝脏是尿素合成的主要器官,肾脏是尿素排泄的主要器官。1932年Krebs等人利用大鼠肝切片作体外实验,发现在供能的条件下,可由CO2和氨合成尿素。若在反应体系中加入少量的精氨酸、鸟氨酸或瓜氨酸可加速尿素的合成,而这种氨基酸的含量并不减少。为此,Krebs等人提出了鸟氨酸循环(ornithine cyclc)学说。其后由Ratner和Cohen详细论述了其各步反应。鸟氨酸循环可概括为:
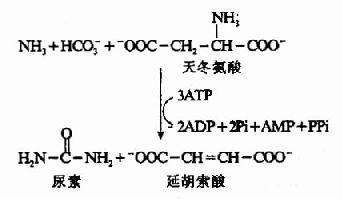
尿素中的两个N原子分别由氨和天冬氨酸提供,而C原子来自HCO-3,五步酶促反应,二步在线粒体中,三步在胞液中进行。其详细过程可分为以下五步:
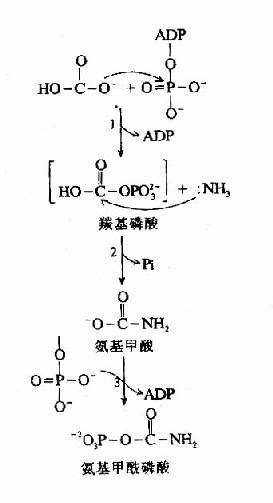
图7-7 CPSⅠ 作用机理
1.氨基甲酰磷酸的合成
氨基甲酰磷酸(carbamylphosphate)是在Mg++、ATP及N乙酰谷氨酸(Nacetyl glutamic acid,AGA)存在的情况下,由氨基甲酰磷酸合成酶I(carbamyl phosphate synthetaseI, CPSI)催化NH3和HCO-3在肝细胞线粒体中合成。
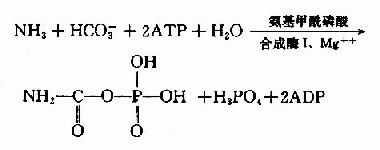
真核细胞中有两种CPS:(1)线粒体CPS-Ⅰ利用游离NH3为氮源合成氨基甲酰磷酸,参与尿素合成。(2)胞液CPS-Ⅱ,利用谷氨酰胺作N源,参与嘧啶的从头合成。
CPS-Ⅰ催化的反应包括下述三步(图7-7)。
(1)ATP活化HCO-3生成ADP和羰基硫酸(carbonyl phosphate)
(2)NH2与羰基硫酸作用替代硫酸根,生成氨基甲酸(carbamate)和Pi。
(3)第2个ATP对氨甲酸磷酸化,生成氨基甲酰磷酸和ADP。
此反应是不可逆的,消耗2分子ATP。CPS1是一种变构酶,AGA是此酶变构激活剂。由乙酰CoA和谷氨酸缩合而成。
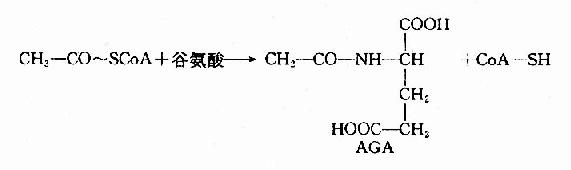
肝细胞线粒体中谷氨酸脱氢酶和氨基甲酰磷酸合成酶I催化的反应是紧密偶联的。谷氨酸脱氢酶催化谷氨酸氧化脱氨,生成的产物有NH3和NADH+H+。NADH经NADH氧化呼吸链传递氧化生成H2O,释放出来的能量用于ADP磷酸化生成ATP。因此谷氨酸脱氢酶催化反应不仅为氨基甲酰磷酸的合成提供了底物NH3,同时也提供了该反应所需要的能量ATP。氨基甲酰磷酸合成酶I将有毒的氨转变成氨基甲酰磷酸,反应中生成的ADP又是谷氨酸脱氢酶的变构激活剂,促进谷氨酸进一步氧化脱氨。这种紧密偶联有利于迅速将氨固定在肝细胞线粒体内,防止氨逸出线粒体进入细胞浆,进而透过细胞膜进入血液,引起血氨升高。
2.瓜氨酸(citrulline)的生成:
乌氨酸氨基甲酰转移酶(ornithinetranscarbamoylase)存在于线粒体中,通常与CPS-I形成酶的复合物催化氨基甲酰磷酸转甲酰基给鸟氨酸生成瓜氨酸。(注意:鸟氨酸,瓜氨酸均非标准α-氨基酸,不出现在蛋白质中)。此反应在线粒体内进行,而鸟氨酸在胞液中生成,所以必需通过一特异的穿棱系统进入线粒体内。

3.精氨酸代琥珀酸(Argininosuccinate)的合成。
瓜氨酸穿过线粒体膜进入胞浆中,在胞浆中由精氨酸代琥珀酸合成酶(Argininosuccinate Synthetase)催化瓜氨酸的脲基与天冬氨酸的氨基缩合生成精氨酸代琥珀酸,获得尿素分子中的第二个氮原子。此反应由ATP供能。
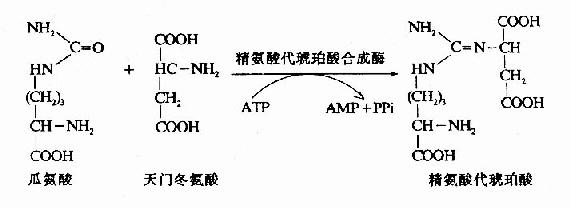
4.精氨酸(Arginine)的生成
精氨酸代琥珀酸裂解酶(Argininosuccinase)催化精氨酸代琥珀酸裂解成精氨酸和延胡索酸
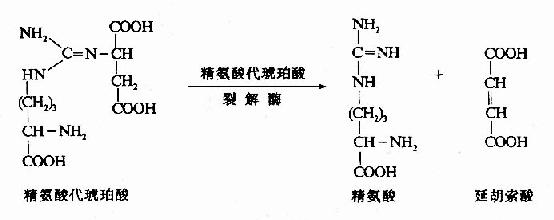
上述反应中生成的延胡索酸可经三羧酸循环的中间步骤生成草酰乙酸,再经谷草转氨酶催化转氨作用重新生成天冬氨酸。由此,通过延胡索酸和天冬氨酸,使三羧酸循环与尿素循环联系起来。
5.尿素的生成
尿素循环的最后一步反应是由精氨酸酶(arginase)催化精氨酸水解生成尿素并再生鸟氨酸,鸟氨酸再进入线粒体参与另一轮循环。
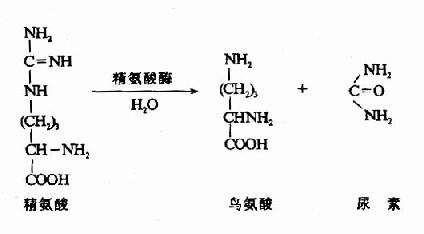
尿素合成是一个耗能的过程,合成1分子尿素需要消耗4个高能磷酸键。(3个ATP水解生成2个ADP,2个Pi,1个AMP和PPi)。从尿素循环底物水平上,能量的消耗大于恢复。由L-谷氨酸脱氢酶催化脱氨和延胡索酸经草酰乙酸再生成天冬氨酸反应中均有NADH的生成。经线粒体再氧化可生成6个ATP(图7-8)。
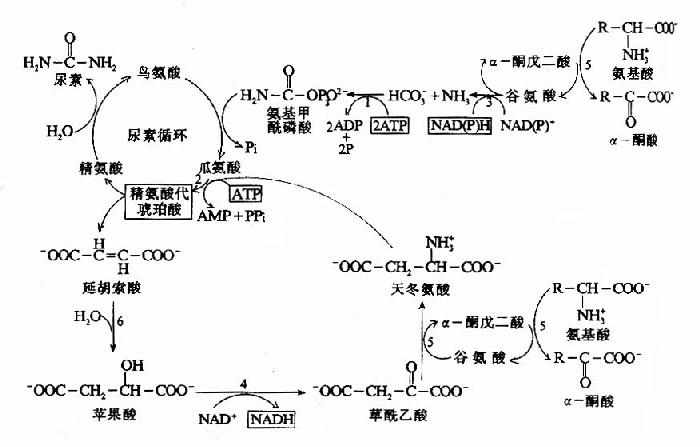
图7-8 尿素循环的能量代谢
6.尿素循环的调节
CPS-I是线粒体内变构酶,其变构激活剂AGA由N乙酰谷氨酸合成酶催化生成,并由特异水解酶水解。肝脏生成尿素的速度与AGA浓度相关。当氨基酸分解旺盛时,由转氨作用引起谷氨酸浓度升高,增加AGA的合成,从而激活CPS-I,加速氨基甲酰磷酸合成,推动尿素循环。精氨酸是AGA合成酶的激活剂,因此,临床利用精氨酸治疗高氨血症。
(五)高氨血症和氨中毒
正常生理情况下,血氨处于较低水平。尿素循环是维持血氨低浓度的关键。当肝功能严重损伤时,尿素循环发生障碍,血氨浓度升高,称为高氨血症。氨中毒机制尚不清楚。一般认为,氨进入脑组织,可与α酮戊二酸结合成谷氨酸,谷氨酸又与氨进一步结合生成谷氨酰胺,从而使α酮戊二酸和谷氨酸减少,导致三羧酸循环减弱,从而使脑组织中ATP生成减少。谷氨酸本身为神经递质,且是另一种神经递质γ-氨基丁酸(γ-aminobutyrate,GABA)的前体,其减少亦会影响大脑的正常生理功能,严重时可出现昏迷。
| 上一页:一、氨基酸的脱氨基作用 |
| 当前页:二、氨的代谢 |
| 下一页:二、α-酮酸的代谢 |